Autor:
Monica Porter
Data De Criação:
22 Marchar 2021
Data De Atualização:
1 Julho 2024

Contente
Porcentagem de massa indica a porcentagem de cada elemento em um composto químico. Para encontrar a porcentagem de massa, deve-se saber a massa molar dos elementos do composto em gramas / mol ou o número de gramas das substâncias que compõem a solução. A porcentagem de massa é calculada usando uma fórmula simples que divide a massa do elemento (ou soluto) pela massa do composto (ou solução).
Passos
Método 1 de 2: Calcule a porcentagem de massa conhecendo a massa
Determine a equação para a porcentagem da massa na mistura. A fórmula básica para calcular a porcentagem de massa na mistura é: porcentagem de massa = (massa de qualidade / massa mista) x 100. Finalmente, você deve multiplicar por 100 para representar a porcentagem.
- Escreva uma equação quando começar a resolver o problema: porcentagem da massa = (massa da substância / massa mista) x 100.
- A quantidade de qualidade será dada no problema. Se o tópico não fornecer, consulte a seção a seguir sobre como encontrar porcentagens de massa sem saber os pesos.
- A massa da mistura é igual à massa total das substâncias que constituem a mistura ou solução.

Calcule a massa da mistura. Depois de saber as massas dos elementos ou compostos, tudo o que você precisa fazer é adicioná-los para obter a massa da mistura ou solução final. Este é o denominador da fórmula para a massa percentual.- Exemplo 1: Qual é a porcentagem em massa de 5 g de hidróxido de sódio quando dissolvido em 100 g de água?
- A massa da mistura é a massa total de hidróxido de sódio e água: 100g + 5g. Portanto, o peso da mistura é 105g.
- Exemplo 2: Que massa de cloreto de sódio e água é necessária para formar 175g de uma solução a 15%?
- Neste exemplo, onde você conhece a massa mista e a porcentagem da massa, a tarefa pede para encontrar a massa do soluto adicionado. A massa da mistura é de 175 g.
- Exemplo 1: Qual é a porcentagem em massa de 5 g de hidróxido de sódio quando dissolvido em 100 g de água?

Determine a massa da substância para encontrar a massa percentual. Quando o questionário pede para encontrar a "porcentagem de massa" de uma substância, você deve encontrar a massa da substância como uma porcentagem da massa total de todos os ingredientes. Escreva a massa da substância para encontrar a massa percentual. Este é o numerador na fórmula da massa percentual.- Exemplo 1: A massa de hidróxido de sódio (substância que pode ser encontrada pela fração de massa) é 5g.
- Exemplo 2: Neste exemplo, a quantidade da substância está procurando a porcentagem da massa desconhecida, e você está procurando por ela.

Substitua as variáveis pela equação das porcentagens de massa. Depois de determinar o valor de cada variável, simplesmente insira-as na equação.- Exemplo 1: porcentagem de massa = (massa da substância / massa mista) x 100 = (5 g / 105 g) x 100.
- Exemplo 2: Precisamos converter a equação de porcentagem de massa para calcular a quantidade de qualidade desconhecida: massa de qualidade = (massa percentual * massa mista) / 100 = (15 * 175) / 100 .
Calcule a porcentagem de volume. Agora que a equação está preenchida, você só precisa calcular a porcentagem de massa. Divida a massa da substância pela massa da mistura e, em seguida, multiplique por 100. Essa é a porcentagem da massa da substância na mistura.
- Exemplo 1: (5/105) x 100 = 0,04761 x 100 = 4,761%. Assim, a percentagem em massa de 5 g de hidróxido de sódio dissolvido em 100 g de água é de 4.761%.
- Exemplo 2: A equação após a conversão para calcular a quantidade de qualidade é (massa percentual * peso misto) / 100: (15 * 175) / 100 = (2625) / 100 = 26,25 gramas Cloreto de Sódio.
- O peso da água adicionada é a massa da mistura menos o peso da substância: 175 - 26,25 = 148,75 gramas de água.
Método 2 de 2: Calcular a porcentagem de massa quando a massa for desconhecida
Determine a equação para a porcentagem da massa no composto. A fórmula básica para calcular a porcentagem da massa em um composto é: porcentagem da massa = (massa molar elementar / massa molar do composto) x 100. A massa molar elementar é a massa de um mol de elemento enquanto a massa molecular é a massa de um mol de composto. Finalmente, você deve multiplicar por 100 para obter o valor da porcentagem.
- Escreva uma equação quando começar a resolver o problema: porcentagem de massa = (massa molar elementar / massa molar do composto) x 100.
- As unidades dos dois valores acima são gramas por mol (g / mol).
- Quando o problema não fornece massa, você pode usar a massa molar para calcular a porcentagem da massa do elemento.
- Exemplo 1: Calcule a porcentagem em massa de hidrogênio em uma molécula de água.
- Exemplo 2: Calcule a porcentagem de massa de carbono em uma molécula de glicose.
Escreva Fórmula química. Se o problema não cobrir as fórmulas químicas de cada composto, você precisará anotá-las. Se o problema for para a fórmula química, pule esta etapa e vá para a etapa "Encontre a massa de cada elemento".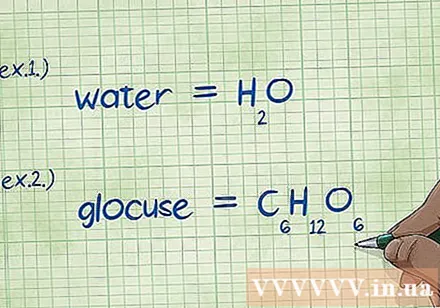
- Exemplo 1: Escreva a fórmula química para água, H2O.
- Exemplo 2: Escreva a fórmula química para glicose, C6H12O6.
Encontre a massa de cada elemento no composto. Procure o peso molecular de cada elemento na fórmula química na tabela periódica. A massa elementar é geralmente escrita abaixo do símbolo químico. Escreva a massa de cada elemento no composto.
- Exemplo 1: Podemos descobrir que o átomo de massa de oxigênio é 15,9994; e o átomo cúbico de hidrogênio é 1.0079.
- Exemplo 2: Descobrimos que o átomo de massa do carbono é 12,0107; o oxigênio é 15.9994; e o hidrogênio é 1,0079.
Multiplique o átomo cúbico pela razão molar. Determine o número de moles (razão molar) de cada elemento no composto químico. A razão molar é calculada pelo pequeno número abaixo na fórmula química do composto. Multiplique o átomo cúbico de cada elemento pela razão molar.
- Exemplo 1: O hidrogênio tem um subscrito de dois, enquanto o oxigênio tem um subscrito de 1. Portanto, multiplique o peso molecular do hidrogênio por 2, 1.00794 X 2 = 2.01588; e a massa molecular do oxigênio é 15.9994 (multiplicada por um).
- Exemplo 2: Carbono tem um subscrito de 6, hidrogênio é 12 e oxigênio é 6. Multiplique o átomo cúbico de cada elemento pelo índice abaixo.
- Carbono (12.0107 * 6) = 72.0642
- Hidrogênio (1.00794 * 12) = 12.09528
- Oxigênio (15,9994 * 6) = 95,9964
Calcule a massa total do composto. Adicione as massas de todos os elementos do composto. Você pode calcular a massa total dos compostos usando as massas calculadas como relações molares. Este número será o denominador na equação da massa percentual.
- Exemplo 1: Adicionar 2.01588 g / mol (a massa de dois moles de átomos de hidrogênio) a 15.9994 g / mol (a massa de um mol de átomos de oxigênio) dá 18.01528 g / mol.
- Exemplo 2: Some todos os pesos juntos: carbono + hidrogênio + oxigênio = 72.0642 + 12.09528 + 95,9964 = 180,156 g / mol.
Determine a massa elementar para a qual a porcentagem da massa deve ser calculada. Quando o problema pede "porcentagem de massa", isso significa que você deve encontrar a massa de um elemento específico no composto como uma porcentagem da massa total de todos os elementos. Determine e anote a massa do elemento. Essa massa é a massa expressa em razão molar. Este número é o numerador da equação percentual da massa.
- Exemplo 1: A massa de hidrogênio em um composto é 2.01588 g / mol (a massa de dois moles de átomos de hidrogênio).
- Exemplo 2: A massa de carbono em um composto é 72.0642 g / mol (a massa de seis moles de átomos de carbono).
Substitua as variáveis pela equação das porcentagens de massa. Após determinar os valores de cada variável, basta substituí-los pela equação identificada na primeira etapa: porcentagem da massa = (massa molar elementar / massa molar do composto) x 100 .
- Exemplo 1: porcentagem de massa = (massa molar elementar / massa molar do composto) x 100 = (2,1588 / 18,1528) x 100.
- Exemplo 2: porcentagem de massa = (massa molar elementar / massa molar do composto) x 100 = (72.0642 / 180.156) x 100.
Calcule a porcentagem de volume. Agora que a equação está preenchida, você só precisa calcular a porcentagem de massa. Divida a massa do elemento pela massa total do composto e, a seguir, multiplique por 100. Essa é a porcentagem da massa do elemento no composto.
- Exemplo 1: porcentagem de massa = (2.01588 / 18.01528) x 100 = 0,111189 x 100 = 11,18%. Assim, a porcentagem de massa do átomo de hidrogênio na molécula de água é 11,18%.
- Exemplo 2: porcentagem de massa = (massa molar elementar / massa molar do composto) x 100 = (72.0642 / 180.156) x 100 = 0,4000 x 100 = 40,00%. Portanto, a porcentagem da massa do átomo de carbono na molécula de glicose é 40,00%.