Autor:
Christy White
Data De Criação:
8 Poderia 2021
Data De Atualização:
1 Julho 2024
Contente
- Dar um passo
- Método 1 de 3: Parte Um: Compreendendo as camadas de elétrons
- Método 2 de 3: Parte Dois: Encontrando Elétrons de Valência em Metais, Exceto Metais de Transição
- Método 3 de 3: Parte Três: Encontrando Elétrons de Valência em Metais de Transição
- Pontas
- Necessidades
Os elétrons de valência ficam na camada externa de um elemento. O número de elétrons de valência em um átomo determina o tipo de ligação química que esse elemento pode formar. A melhor maneira de descobrir o número de elétrons de valência é usar a tabela periódica dos elementos.
Dar um passo
Método 1 de 3: Parte Um: Compreendendo as camadas de elétrons
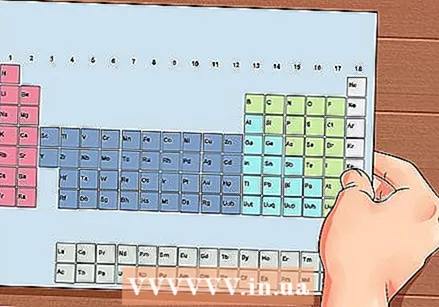 A Tabela Periódica dos Elementos. Esta é uma tabela com códigos de cores, onde em cada célula um elemento é mostrado com o número atômico e 1 a 3 letras como símbolo.
A Tabela Periódica dos Elementos. Esta é uma tabela com códigos de cores, onde em cada célula um elemento é mostrado com o número atômico e 1 a 3 letras como símbolo. 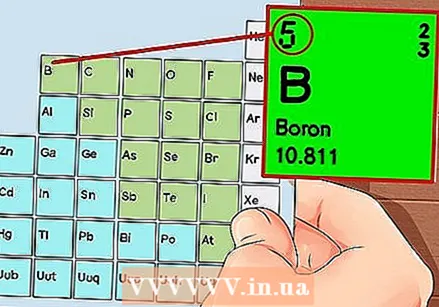 Encontre o número atômico do elemento. O número atômico está acima ou próximo ao símbolo do elemento. Por exemplo: Boro (B) possui um número atômico 5, o que significa que possui 5 prótons e 5 elétrons.
Encontre o número atômico do elemento. O número atômico está acima ou próximo ao símbolo do elemento. Por exemplo: Boro (B) possui um número atômico 5, o que significa que possui 5 prótons e 5 elétrons. 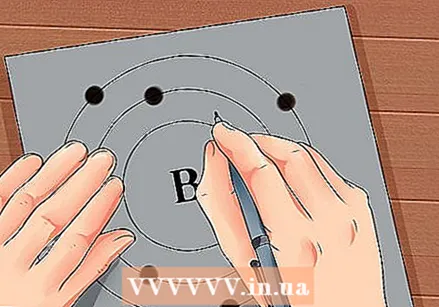 Desenhe uma representação simples de um átomo e coloque os elétrons em órbita ao redor do núcleo. Esses trabalhos também são chamados de conchas ou níveis de energia. O número máximo de elétrons que podem estar na mesma camada é fixo e as camadas são preenchidas da órbita interna para a externa.
Desenhe uma representação simples de um átomo e coloque os elétrons em órbita ao redor do núcleo. Esses trabalhos também são chamados de conchas ou níveis de energia. O número máximo de elétrons que podem estar na mesma camada é fixo e as camadas são preenchidas da órbita interna para a externa. - K Shell (interno): 2 elétrons no máximo.
- L Shell: 8 elétrons no máximo.
- Shell M: máximo de 18 elétrons.
- N Shell: 32 elétrons no máximo.
- O Shell: máximo de 50 elétrons.
- P Shell (externo): 72 elétrons no máximo.
 Encontre o número de elétrons na camada externa. Esses são os elétrons de valência.
Encontre o número de elétrons na camada externa. Esses são os elétrons de valência. - Quando a camada de valência está cheia, o elemento é estável.
- Se a camada de valência não estiver cheia, o elemento é reativo, o que significa que ele pode se ligar quimicamente ao átomo de outro elemento. Cada átomo compartilha seus elétrons de valência em uma tentativa de preencher a camada de valência.
Método 2 de 3: Parte Dois: Encontrando Elétrons de Valência em Metais, Exceto Metais de Transição
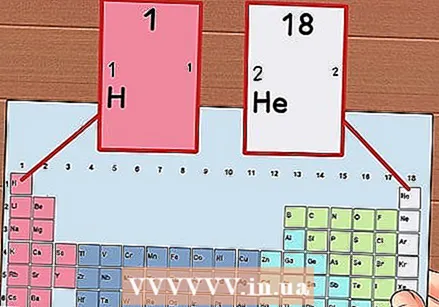 Numere cada coluna da tabela periódica, de 1 a 18. O hidrogênio (H) está no topo da coluna 1 e o Hélio (He) no topo da coluna 18. Esses são os diferentes grupos de elementos.
Numere cada coluna da tabela periódica, de 1 a 18. O hidrogênio (H) está no topo da coluna 1 e o Hélio (He) no topo da coluna 18. Esses são os diferentes grupos de elementos. 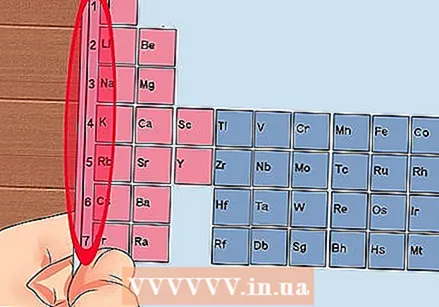 Dê a cada linha um número, de 1 a 7. Esses são os períodos dos elementos e correspondem ao número de camadas ou níveis de energia de um átomo.
Dê a cada linha um número, de 1 a 7. Esses são os períodos dos elementos e correspondem ao número de camadas ou níveis de energia de um átomo. - Hidrogênio (H) e Hélio (He) têm 1 camada, enquanto Francium (Fr) tem 7.
- Os lantanídeos e actinídeos são agrupados e listados abaixo da tabela principal. Todos os lantanídeos pertencem ao Período 6, Grupo 3 e todos os actinídeos pertencem ao Período 7, Grupo 3.
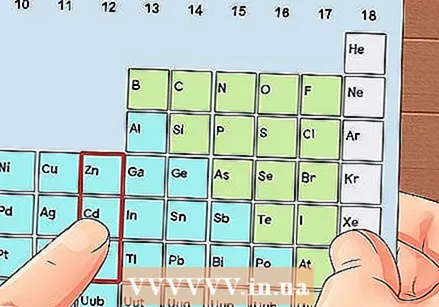 Localize um elemento que não seja um metal de transição. Os metais de transição estão nos grupos de 3 a 12. Os números dos grupos dos outros metais indicam o número de elétrons de valência.
Localize um elemento que não seja um metal de transição. Os metais de transição estão nos grupos de 3 a 12. Os números dos grupos dos outros metais indicam o número de elétrons de valência. - Grupo 1: 1 elétron de valência
- Grupo 2: 2 elétrons de valência
- Grupo 13: 3 elétrons de valência
- Grupo 14: 4 elétrons de valência
- Grupo 15: 5 elétrons de valência
- Grupo 16: 6 elétrons de valência
- Grupo 17: 7 elétrons de valência
- Grupo 18: 8 elétrons de valência - exceto Hélio, que tem 2
Método 3 de 3: Parte Três: Encontrando Elétrons de Valência em Metais de Transição
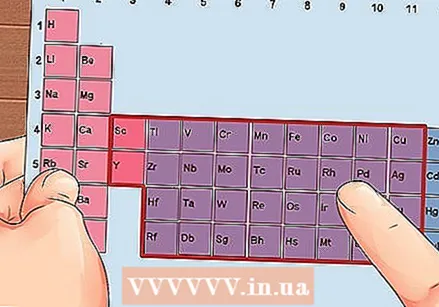 Encontre um elemento dos grupos 3 a 12, os metais de transição.
Encontre um elemento dos grupos 3 a 12, os metais de transição. Determine o número de elétrons de valência com base no número do grupo. Esses números de grupo correspondem a um possível número de elétrons de valência.
Determine o número de elétrons de valência com base no número do grupo. Esses números de grupo correspondem a um possível número de elétrons de valência. - Grupo 3: 3 elétrons de valência
- Grupo 4: 2 a 4 elétrons de valência
- Grupo 5: 2 a 5 elétrons de valência
- Grupo 6: 2 a 6 elétrons de valência
- Grupo 7: 2 a 7 elétrons de valência
- Grupo 8: 2 ou 3 elétrons de valência
- Grupo 9: 2 ou 3 elétrons de valência
- Grupo 10: 2 ou 3 elétrons de valência
- Grupo 11: 1 ou 2 elétrons de valência
- Grupo 12: 2 elétrons de valência
Pontas
- Os metais de transição podem ter conchas de valência que não estão completamente cheias. Determinar o número exato de elétrons de valência em metais de transição requer certos princípios da teoria quântica que estão além do escopo deste artigo.
Necessidades
- Tabela periódica dos elementos
- Lápis
- Papel