Autor:
Frank Hunt
Data De Criação:
13 Marchar 2021
Data De Atualização:
1 Julho 2024

Contente
- Dar um passo
- Método 1 de 3: usando um medidor de pH
- Método 2 de 3: com papel de tornassol
- Método 3 de 3: Compreendendo o pH
É importante medir o pH - o grau de acidez ou alcalinidade - da água. A água é usada pelas plantas e animais de que dependemos e a bebemos todos os dias. O valor do pH da água pode ser uma indicação de possível contaminação, portanto, medir o pH da água pode ser uma importante precaução de saúde pública.
Dar um passo
Método 1 de 3: usando um medidor de pH
 Calibre a sonda e o medidor de acordo com as instruções de fábrica. Pode ser necessário calibrar o medidor usando uma substância com um valor de pH conhecido. O medidor pode ser ajustado de acordo com essa substância. Se você for testar a água fora de um laboratório, é recomendável realizar esta calibração algumas horas antes do teste de campo.
Calibre a sonda e o medidor de acordo com as instruções de fábrica. Pode ser necessário calibrar o medidor usando uma substância com um valor de pH conhecido. O medidor pode ser ajustado de acordo com essa substância. Se você for testar a água fora de um laboratório, é recomendável realizar esta calibração algumas horas antes do teste de campo. - Enxágue a sonda com água limpa antes de usar. Seque com um pano limpo.
 Pegue uma amostra de água e despeje em um recipiente limpo.
Pegue uma amostra de água e despeje em um recipiente limpo.- A água deve ser profunda o suficiente para submergir a ponta do eletrodo.
- Deixe a amostra por um tempo para permitir que a temperatura se estabilize.
- Meça a temperatura da amostra com um termômetro.
 Ajuste o medidor com a temperatura da amostra. A sensibilidade da sonda é afetada pela temperatura da água, portanto a medição só pode ser precisa se você inserir os dados de temperatura.
Ajuste o medidor com a temperatura da amostra. A sensibilidade da sonda é afetada pela temperatura da água, portanto a medição só pode ser precisa se você inserir os dados de temperatura.  Coloque a sonda na amostra. Aguarde até que o medidor alcance o equilíbrio. O medidor está em um estado estacionário quando a leitura está estável.
Coloque a sonda na amostra. Aguarde até que o medidor alcance o equilíbrio. O medidor está em um estado estacionário quando a leitura está estável.  Leia a medição de pH da amostra. O medidor de pH dá o resultado em uma escala de 0-14. Se a água for pura, o valor é em torno de 7. Anote suas descobertas.
Leia a medição de pH da amostra. O medidor de pH dá o resultado em uma escala de 0-14. Se a água for pura, o valor é em torno de 7. Anote suas descobertas.
Método 2 de 3: com papel de tornassol
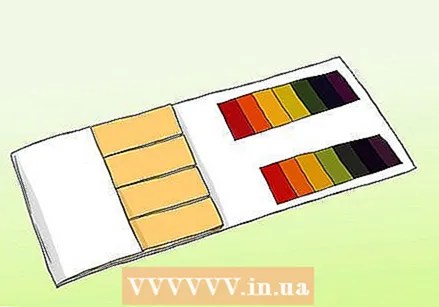 Aprenda a diferença entre papel de pH e papel de tornassol. Você pode usar papel de pH para obter uma leitura precisa de uma amostra. No entanto, o papel de pH não deve ser confundido com o papel de tornassol regular. Ambos podem ser usados para testar ácidos e bases, mas diferem em aspectos importantes.
Aprenda a diferença entre papel de pH e papel de tornassol. Você pode usar papel de pH para obter uma leitura precisa de uma amostra. No entanto, o papel de pH não deve ser confundido com o papel de tornassol regular. Ambos podem ser usados para testar ácidos e bases, mas diferem em aspectos importantes. - As tiras de pH contêm uma série de barras indicadoras que mudam de cor quando expostas a uma solução. A força dos ácidos e bases em cada barra é diferente. Após a alteração, o padrão de cores pode ser comparado com as amostras fornecidas com o kit.
- O papel de tornassol é uma tira de papel que contém um ácido ou base (alcalino). As listras mais comuns são vermelhas (com um ácido que reage com as bases) e azul (com uma base que reage com ácidos). As listras vermelhas ficam azuis se a substância for alcalina e as listras azuis ficam vermelhas se a substância for ácida. Papéis tornassol podem ser usados como um teste rápido e fácil, mas as variedades mais baratas nem sempre fornecem uma medida precisa da força da solução.
 Pegue uma amostra da água e despeje em um recipiente limpo. A água deve ser profunda o suficiente para submergir a faixa.
Pegue uma amostra da água e despeje em um recipiente limpo. A água deve ser profunda o suficiente para submergir a faixa.  Mergulhe uma tira de teste na amostra. A exposição de alguns segundos é o suficiente. As barras indicadoras no papel mudarão de cor após alguns momentos.
Mergulhe uma tira de teste na amostra. A exposição de alguns segundos é o suficiente. As barras indicadoras no papel mudarão de cor após alguns momentos.  Compare o final da tira de teste com a tabela de cores que veio com o papel. A cor ou cores do cartão devem coincidir com a cor ou cores da tira de teste. O mapa de cores relaciona os padrões de cores aos níveis de pH.
Compare o final da tira de teste com a tabela de cores que veio com o papel. A cor ou cores do cartão devem coincidir com a cor ou cores da tira de teste. O mapa de cores relaciona os padrões de cores aos níveis de pH.
Método 3 de 3: Compreendendo o pH
 Aprenda como ácidos e bases são definidos. A acidez e a alcalinidade (o termo usado para descrever as bases) são definidas pelos íons de hidrogênio que elas doam ou absorvem. Um ácido é uma substância que doa (ou "doa") íons de hidrogênio, e uma base é uma substância que absorve íons de hidrogênio extras.
Aprenda como ácidos e bases são definidos. A acidez e a alcalinidade (o termo usado para descrever as bases) são definidas pelos íons de hidrogênio que elas doam ou absorvem. Um ácido é uma substância que doa (ou "doa") íons de hidrogênio, e uma base é uma substância que absorve íons de hidrogênio extras.  Compreenda a escala de pH. O número de pH é usado para medir o grau de acidez ou alcalinidade de substâncias solúveis em água. A água normalmente tem a mesma quantidade de íons hidróxido (OH−) e íons hidrônio (H3O +). A proporção de íons hidróxido e hidrônio muda quando uma substância ácida ou alcalina é adicionada à água.
Compreenda a escala de pH. O número de pH é usado para medir o grau de acidez ou alcalinidade de substâncias solúveis em água. A água normalmente tem a mesma quantidade de íons hidróxido (OH−) e íons hidrônio (H3O +). A proporção de íons hidróxido e hidrônio muda quando uma substância ácida ou alcalina é adicionada à água. - Geralmente é considerada uma escala que vai de 0 a 14 (embora as substâncias possam estar fora dessa faixa). Substâncias neutras têm pontuação de cerca de 7, substâncias ácidas estão abaixo de 7 e substâncias alcalinas acima de 7.
- A escala de pH é logarítmica, o que significa que diferenças inteiras representam uma diferença de dez vezes na acidez ou alcalinidade. Por exemplo, uma substância com pH 2 é dez vezes mais ácida do que uma substância com pH 3 e 100 vezes mais ácida do que uma substância com pH 4. A escala funciona da mesma forma com substâncias alcalinas, com qualquer sendo inteiro representa uma diferença de dez vezes.
 Saiba por que testamos o pH da água. A água pura tem um pH de 7, mas a água da torneira holandesa geralmente tem um pH entre 7,5 e 8,3. Água muito ácida (água com baixo valor de pH) tem maior probabilidade de dissolver produtos químicos tóxicos. Isso pode poluir a água e torná-la imprópria para beber.
Saiba por que testamos o pH da água. A água pura tem um pH de 7, mas a água da torneira holandesa geralmente tem um pH entre 7,5 e 8,3. Água muito ácida (água com baixo valor de pH) tem maior probabilidade de dissolver produtos químicos tóxicos. Isso pode poluir a água e torná-la imprópria para beber. - Em geral, é aconselhável testar o pH no local. Se você coletar uma amostra de água para pesquisa de laboratório, o dióxido de carbono (CO2) do ar pode se dissolver na água. O dióxido de carbono dissolvido reage com os íons na água e aumenta a acidez em soluções básicas ou neutras. Para evitar a contaminação por dióxido de carbono, a água deve ser testada dentro de duas horas após a coleta.



